Felles wrote:
Volodymyr wrote:
Зачем изобретать велосипед?
В каком смысле? У меня нет соляной кислоты, я ищу максимально простой способ ее получения.
То есть, мне придется все-таки нагревать смесь?
Или может так подгадать,чтобы вся серная кислота прореагировала, а в растворе осталась соляная? (Если я вас правильно понял)
Не получится.
Сейчас идет зима, то можно получить соляную кислоту прямой перегонкой соли с электролитом, на снежной бане. .
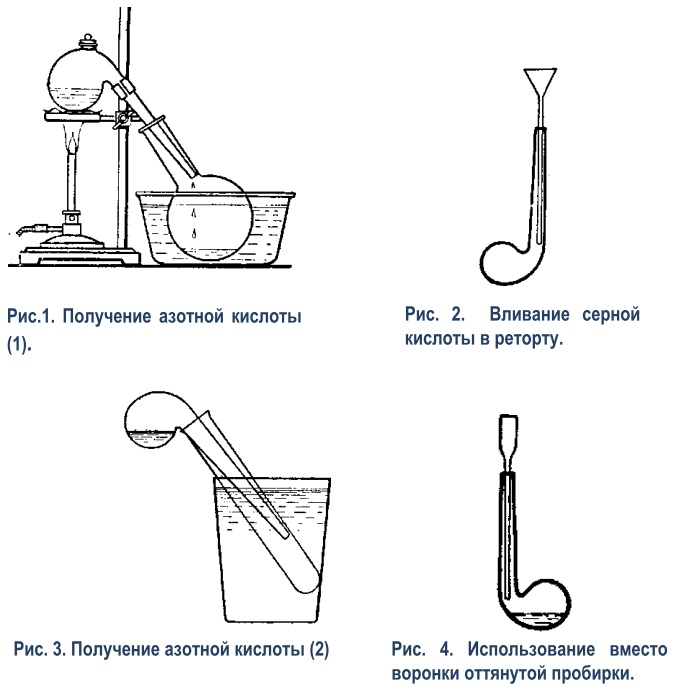
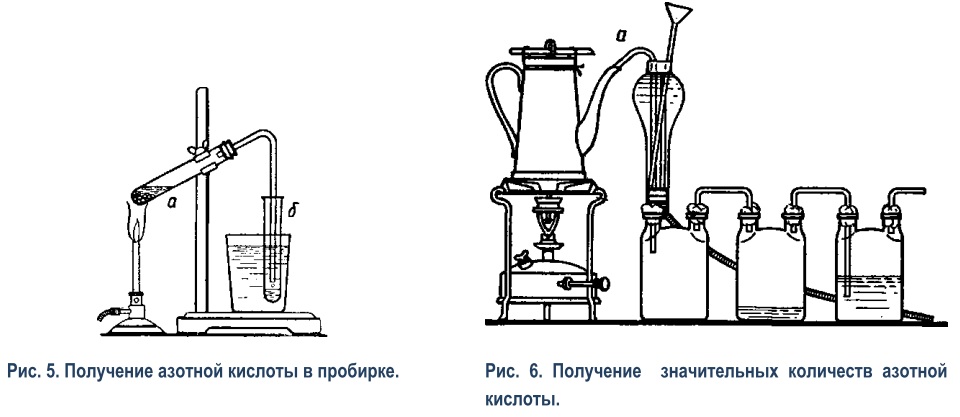
На 340 г (пересчитайте в мл сами) серной кислоты добавте 120г повареной соли, растворить соль до предела. и затем перегнать до предела, что бы на дне оставалась почти сухая соль.Перегоняйте таким аппаратом, на медленном огне, иначе будет пенитья.
Тут образуется азеотроп хлористого водорода с водой, (ок 20% HCl), еще и процесс высаливания. Должна получится кислота ок 20%.: В приемную колбу будет идти уже соляная кислота. Возможно первые пары будут содержать много газообразного HCl, то колбу изнутри немного смочить.
| Attachments: |
|
1.PNG [ 9.38 KiB | Viewed 18698 times ] |